pour la recherche uniquement
Prucalopride Succinate 5-HT Receptor agoniste
Réf. CatalogueS4247
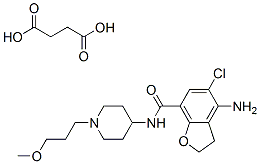
Structure chimique
Poids moléculaire: 485.96
Contrôle Qualité
| Cibles apparentées | Adrenergic Receptor AChR COX Calcium Channel Histamine Receptor Dopamine Receptor GABA Receptor TRP Channel Cholinesterase (ChE) GluR |
|---|---|
| Autre 5-HT Receptor Inhibiteurs | WAY-100635 Maleate Serotonin (5-HT) HCl Puerarin BRL-15572 Dihydrochloride SB269970 HCl Ketanserin RS-127445 Nuciferine Flopropione BRL-54443 |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 485.96 | Formule | C18H26ClN3O3.C4H6O4 |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 179474-85-2 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | R-108512 | Smiles | COCCCN1CCC(CC1)NC(=O)C2=CC(=C(C3=C2OCC3)N)Cl.C(CC(=O)O)C(=O)O | ||
Solubilité
|
In vitro |
DMSO
: 97 mg/mL
(199.6 mM)
Water : 97 mg/mL Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
5-HT4A
2.5 nM(Ki)
5-HT4B
8 nM(Ki)
|
|---|---|
| In vitro |
Le Prucalopride induit des contractions de manière concentration-dépendante avec un pEC50 de 7,5. Le Prucalopride (1 mM) amplifie significativement la contraction de rebond du côlon proximal de cobaye après stimulation par champ électrique. Le Prucalopride induit une relaxation de la préparation de la tunica muscularis mucosae de l'œsophage de rat avec un pEC50 de 7,8, donnant une courbe concentration-réponse monophasique. Le Prucalopride (0,1 μM) augmente de manière concentration-dépendante l'amplitude des contractions cholinergiques sous-maximales et de la libération d'acétylcholine induites par la stimulation par champ électrique dans le muscle circulaire gastrique de porc, et l'effet est induit et amélioré par l'IBMX (10 μM). Le Prucalopride (1 μM) améliore significativement les contractions cholinergiques induites électriquement dans le côlon descendant de porc, et l'effet facilitateur est significativement amélioré par le Rolipram. |
| In vivo |
Le Prucalopride modifie les profils de motilité contractile du côlon de manière dose-dépendante en stimulant des contractions groupées de haute amplitude dans le côlon proximal et en inhibant l'activité contractile dans le côlon distal de chiens à jeun. Le Prucalopride provoque également une diminution dose-dépendante du temps jusqu'à la première contraction migratoire géante (CMG) ; à des doses plus élevées de prucalopride, la première CMG survient généralement dans la première demi-heure après le traitement. |
Références |
|
Informations sur lessai clinique
(données du https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Promoteur/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT04838522 | Recruiting | Chronic Constipation |
Takeda|UC San Diego Human Milk Research Biorepository |
March 2 2022 | -- |
| NCT04429802 | Completed | Gastrointestinal Motility Disorder|Dyspepsia |
Universitaire Ziekenhuizen KU Leuven |
September 26 2013 | Not Applicable |
| NCT01807000 | Completed | Healthy |
Shire|Takeda |
March 18 2013 | Phase 1 |
| NCT01692132 | Withdrawn | Chronic Constipation |
Janssen Pharmaceutica |
February 2013 | -- |
| NCT03279341 | Completed | Chronic Constipation |
University Hospital Gasthuisberg |
December 3 2012 | Phase 4 |
| NCT01117051 | Terminated | Non-cancer Pain|Opioid Induced Constipation |
Shire|Takeda |
May 19 2010 | Phase 3 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
