pour la recherche uniquement
TTNPB (Arotinoid acid) Agoniste RAR
Réf. CatalogueS4627
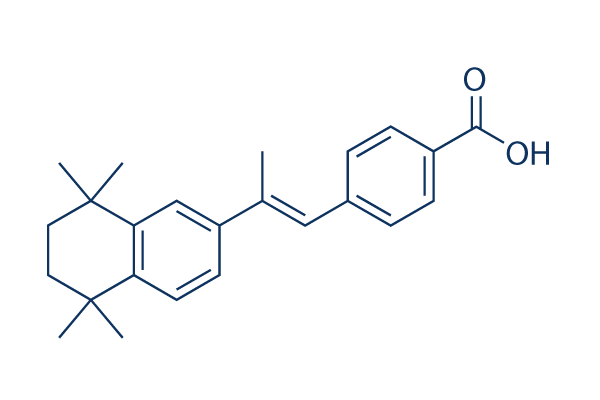
Structure chimique
Poids moléculaire: 348.48
Contrôle Qualité
| Cibles apparentées | Dehydrogenase HSP Transferase P450 (e.g. CYP17) PDE phosphatase PPAR Vitamin Carbohydrate Metabolism Mitochondrial Metabolism |
|---|---|
| Autre Retinoid Receptor Inhibiteurs | Tamibarotene AM580 Fenretinide UVI 3003 SR 11237 AR7 BMS493 All trans-Retinal MSU-42011 Palovarotene |
Culture cellulaire, traitement et concentration de travail
| Lignées cellulaires | Type dessai | Concentration | Temps dincubation | Formulation | Description de lactivité | PMID |
|---|---|---|---|---|---|---|
| HEK293 cells | Function assay | Agonist activity at human RARalpha expressed in HEK293 cells by luciferase reporter gene assay, EC50=0.18 nM | ||||
| CV-1 cells | Function assay | Binding affinity against retinoic Acid gamma receptors co-transfected into CV-1 cells, EC50=0.002 Μm | ||||
| HL60 cells | Cytotoxicity assay | In vitro cytotoxicity against HL60 cells, IC50=46 μM | ||||
| HeLa cells | Function assay | Agonist activity at human RARalpha expressed in human HeLa cells assessed as relative luminescence units at >=10 uM by luciferase assay relative to control | ||||
| Cliquez pour voir plus de données expérimentales sur la lignée cellulaire | ||||||
Informations chimiques, stockage et stabilité
| Poids moléculaire | 348.48 | Formule | C24H28O2 |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 71441-28-6 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | Arotinoid Acid, Ro 13-7410, AGN-191183 | Smiles | CC(=CC1=CC=C(C=C1)C(=O)O)C2=CC3=C(C=C2)C(CCC3(C)C)(C)C | ||
Solubilité
|
In vitro |
DMSO
: 15 mg/mL
(43.04 mM)
Water : Insoluble Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
RARβ
(cell-free assay) 4.5 nM
RARα
(cell-free assay) 5.1 nM
RARγ
(cell-free assay) 9.3 nM
|
|---|---|
| In vitro |
TTNPB se lie aux Retinoid Receptor nucléaires avec une haute affinité, et inhibe la liaison du [3H]tRA avec une IC50 de 3,8 nM, 4,0 nM, et 4,5 nM pour mRARα, β, et γ, respectivement. Ce composé augmente l'activation transcriptionnelle des RAR de souris dans les cellules JEG-3 après 72 h en utilisant un milieu conditionné avec une EC50 de 2,0 nM, 1,1 nM et 0,8 nM pour mRARα, β, et γ, respectivement. Il inhibe la croissance des cellules épithéliales mammaires humaines normales (HMECs) et des cellules de cancer du sein positives aux récepteurs d'œstrogènes (ER-positives) en induisant un blocage du cycle cellulaire en phase G1. Ce produit chimique provoque une diminution dose-dépendante de la différenciation des cellules ES-D3.
|
| Essai kinase |
Essais de liaison
|
|
Les essais de liaison sont effectués comme décrit précédemment (Allenby et al., 1993, 1994). En bref, les rétinoïdes marqués et non marqués sont ajoutés aux fractions nucléosol ou cytosoliques dans l'éthanol de manière à ce que la quantité totale d'éthanol ajoutée soit constante dans tous les tubes et ne dépasse pas 2 % du volume d'incubation. Les préparations de récepteurs sont incubées avec des rétinoïdes à 4 °C pendant 4 à 6 heures. Des colonnes de dessalement Sephadex PD-10 sont utilisées pour séparer le radioligand lié du radioligand libre une fois l'équilibre atteint. Pour les essais de liaison compétitive, des concentrations variables de ligand compétitif non marqué sont incubées avec le nucléosol ou le cytosol approprié en présence d'une concentration fixe de [3H]tRA (act. sp. 49,3 Ci/mmol) ou de [3H]9-cis RA (act. sp. 24,0 Ci/mmol). Les concentrations finales de [3H]tRA et [3H]9-cis RA pour les essais de liaison aux Retinoid Receptor nucléaires sont de 5 nM. Les concentrations finales de [3H]tRA pour les essais de liaison au CRABP sont de 30 nM. Les IC50 sont calculées comme décrit ci-dessus (DeLean et al., 1978). Pour la cinétique de saturation, des concentrations croissantes de ligand radiomarqué ([3H]tRA act. sp. 49,3 Ci/mmol, [3H]this compound act. sp. 5,5 Ci/mmol) sont ajoutées au nucléosol du sous-type de récepteur approprié en présence (liaison non spécifique) ou en absence (liaison totale) d'un excès molaire de 100 fois du rétinoïde non marqué correspondant. La liaison spécifique est définie comme la liaison totale moins la liaison non spécifique. La cinétique de saturation est calculée comme décrit précédemment (Scatchard, 1949; Grippo et Gudas, 1987; Levin et al., 1992).
|
|
| In vivo |
TTNPB (0,25 mg/kg) provoque une inhibition de la croissance dans les deux modèles MXT-HS et MXT-HI en induisant l'apoptose cellulaire.
|
Références |
|
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
