pour la recherche uniquement
AEE788 (NVP-AEE788) EGFR inhibiteur
Réf. CatalogueS1486
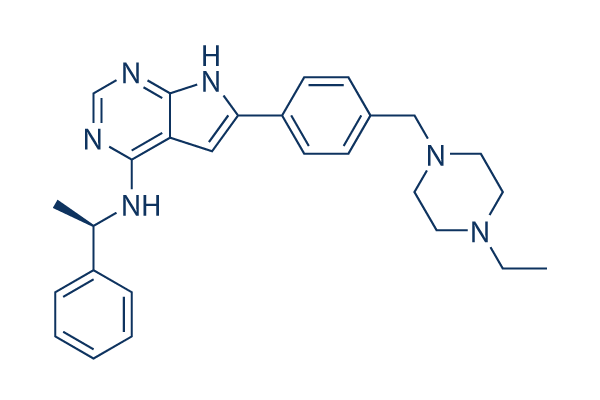
Structure chimique
Poids moléculaire: 440.58
Contrôle Qualité
| Cibles apparentées | VEGFR PDGFR FGFR c-Met Src MEK CSF-1R FLT3 HER2 c-Kit |
|---|---|
| Autre EGFR Inhibiteurs | Lazertinib (YH25448) Icotinib Hydrochloride Sunvozertinib AG-490 AG-1478 Canertinib (CI-1033) WZ4002 Rociletinib (CO-1686) Poziotinib (NOV120101, HM781-36B) Genistein |
Culture cellulaire, traitement et concentration de travail
| Lignées cellulaires | Type dessai | Concentration | Temps dincubation | Formulation | Description de lactivité | PMID |
|---|---|---|---|---|---|---|
| Huh7 | Cytotoxicity assay | Cytotoxicity against human hepatocellular carcinoma cell line (Huh7), CC50=27.83 Μm | ||||
| Jeko B cells | Function assay | 2 h | Inhibition of PI3Kdelta in human Jeko B cells assessed as inhibition of Akt phosphorylation after 2 hrs, IC50=0.017 μM | |||
| Cliquez pour voir plus de données expérimentales sur la lignée cellulaire | ||||||
Informations chimiques, stockage et stabilité
| Poids moléculaire | 440.58 | Formule | C27H32N6 |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 497839-62-0 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | N/A | Smiles | CCN1CCN(CC1)CC2=CC=C(C=C2)C3=CC4=C(N3)N=CN=C4NC(C)C5=CC=CC=C5 | ||
Solubilité
|
In vitro |
DMSO
: 88 mg/mL
(199.73 mM)
Water : Insoluble Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
EGFR
(Cell-free assay) 2 nM
HER2/ErbB2
(Cell-free assay) 6 nM
c-Abl
(Cell-free assay) 52 nM
FLT1
(Cell-free assay) 59 nM
c-Fms
(Cell-free assay) 60 nM
c-Src
(Cell-free assay) 61 nM
KDR
(Cell-free assay) 77 nM
HER4/ErbB4
(Cell-free assay) 160 nM
|
|---|---|
| In vitro |
AEE788 (NVP-AEE788) inhibe également KDR, c-abl, c-Src et Flt-1 avec des IC50 de 50-80 nM. Il n'est pas sensible à ErbB-4, PDGFR-β, Flt-3, Flt-4, RET et c-Kit et n'a pas d'effet inhibiteur sur Ins-R, IGF-1R, PKC-α et PKA. Ce composé inhibe puissamment la phosphorylation d'EGFR dans les cellules A431 avec une IC50 de 11 nM. Il inhibe également la phosphorylation de KDR dans les cellules CHO et d'erbB2 dans les cellules BT-474, sans aucun effet sur la phosphorylation induite par le PDGF dans les cellules A31. Il inhibe la prolifération des cellules NCI-H596, MK, BT-474 et SK-BR-3 avec des IC50 de 78, 56, 49 et 381 nM, respectivement. Par ailleurs, il possède la propriété supplémentaire d'inhiber la prolifération cellulaire induite par le mutant d'EGFR, y compris 32D/EGFR et 32D/EGFRvIII. Il inhibe en outre la prolifération des HUVEC induite par l'EGF et le VEGF avec des IC50 de 43 et 155 nM, respectivement. Il inhibe la phosphorylation d'EGFR, VEGFR2, Akt et MAPK dans les lignées cellulaires humaines de carcinome épidermoïde cutané (cellules Colo16, HaCaT, SRB1 et SRB12), ce qui entraîne une inhibition de la croissance et une induction de l'apoptose. Il inhibe la phosphorylation d'EGFR et d'Akt dans les cellules HT29 à des concentrations de 0,2 à 1,0 μM. Il inhibe la prolifération cellulaire et prévient l'activation de HER1, HER2 et HER3 induite par l'EGF et la neuréguline dans les lignées cellulaires de médulloblastome. Il présente des activités suppressives de croissance dans les cellules de médulloblastome chimiosensibles et chimiorésistantes.
|
| Essai kinase |
Tests de Protein Kinase
|
|
Les tests in vitro de Protein Tyrosine Kinase pour AEE788 (NVP-AEE788) sont réalisés dans des plaques à 96 puits (30 μL) à température ambiante pendant 15 à 45 min en utilisant les domaines kinase recombinants fusionnés à la glutathion S-transférase (4-100 ng, selon l'activité spécifique). Le [γ33P]ATP est utilisé comme donneur de phosphate et le peptide polyGluTyr-(4:1) comme accepteur. À l'exception de la Protein Kinase C-α, la cycline-dépendante kinase 1/cycB et la Protein Kinase A, le sulfate de protamine (200 μg/mL), l'histone H1 (100 μg/mL) et l'heptapeptide Leu-Arg-Arg-Ala-Ser-Leu-Gly (connu sous le nom de Kemptide Bachem) sont respectivement utilisés comme substrats peptidiques. Les tests sont optimisés pour chaque kinase en utilisant les concentrations d'ATP suivantes : 1,0 μM (c-Kit, c-Met, c-Fms, c-Raf-1 et RET), 2,0 μM (EGFR, erbB2, ErbB3 et ErbB4), 5,0 μM (c-abl), 8,0 μM (Flt-1, Flt-3, Flt-4, Flk, KDR, FGFR-1 et Tek), 10,0 μM (PDGFR-β, Protein Kinase C-α et cycline-dépendante kinase 1) et 20,0 μM (c-Src et Protein Kinase A). La réaction est terminée par l'ajout de 20 μL d'EDTA 125 mM. Trente μL (c-abl, c-Src, récepteur du facteur de croissance 1 de l'insuline, RET-Men2A et RET-Men2B) ou 40 μL (toutes les autres kinases) du mélange réactionnel sont transférés sur une membrane Immobilon-polyvinylidène difluorure, pré-trempée avec 0,5% H3PO4 et montée sur un collecteur de vide. Le vide est ensuite appliqué et chaque puits rincé avec 200 μL de H3PO4 à 0,5%. Les membranes sont retirées et lavées quatre fois avec 1,0% H3PO4 et une fois avec de l'éthanol. Les membranes séchées sont comptées après montage dans un cadre Packard TopCount à 96 puits et avec l'ajout de 10 μL/puits de Microscint. Les valeurs d'IC50 (±SE) sont calculées par analyse de régression linéaire du pourcentage d'inhibition et sont des moyennes d'au moins trois déterminations.
|
|
| In vivo |
AEE788 (NVP-AEE788) produit une inhibition dose-dépendante de la croissance tumorale dans les modèles de xénogreffe NCI-H596 ou DU145, avec seulement des changements mineurs du poids corporel. Il induit une régression tumorale de 57% à 50 mg/kg dans le modèle NeuT/erbB2 GeMag et inhibe puissamment la phosphorylation de l'EGFR induite par l'EGF dans les tumeurs A431 et la phosphorylation d'erbB2 dans les tumeurs GeMag. Ce composé inhibe de manière dose-dépendante l'angiogenèse induite par le VEGF et n'inhibe pas l'angiogenèse induite par le bFGF. Il supprime la croissance du volume tumoral de 54% dans les xénogreffes Colo16 à 50 mg/kg, ce qui est dû à l'inhibition de la phosphorylation d'EGFR, VEGFR, Akt et MAPK. À 50 mg/kg, il inhibe également la croissance des tumeurs dans le cæcum et le péritoine (>50%) et réduit l'incidence des métastases ganglionnaires à 70% dans les cellules HT29 implantées dans le cæcum de souris nues, sans perte de poids corporel et sans preuve macroscopique de néovascularisation. Il abaisse significativement les niveaux d'expression de pEGFR et pVEGFR dans les tumeurs cæcales HT29 et ne modifie pas ceux d'EGF, VEGF, EGFR ou VEGFR. Combiné avec le CPT-11, il entraîne des tumeurs significativement plus petites et une inhibition complète des métastases ganglionnaires. Ce composé inhibe la croissance des xénogreffes Daoy, DaoyPt et DaoyHER2 de 51%, 45% et 72%, respectivement. Il pourrait promouvoir la génération d'espèces réactives de l'oxygène médiée par LBH589 dans les cellules tumorales K562, ce qui à son tour augmente l'apoptose.
|
Références |
|
Informations sur lessai clinique
(données du https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Promoteur/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT00107237 | Completed | Brain and Central Nervous System Tumors |
Novartis Pharmaceuticals|Novartis |
October 2003 | Phase 1|Phase 2 |
| NCT00118456 | Completed | Cancer |
Novartis Pharmaceuticals|Novartis |
July 2003 | Phase 1 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
