pour la recherche uniquement
Cidofovir DNA/RNA Synthesis inhibiteur
Réf. CatalogueS1516
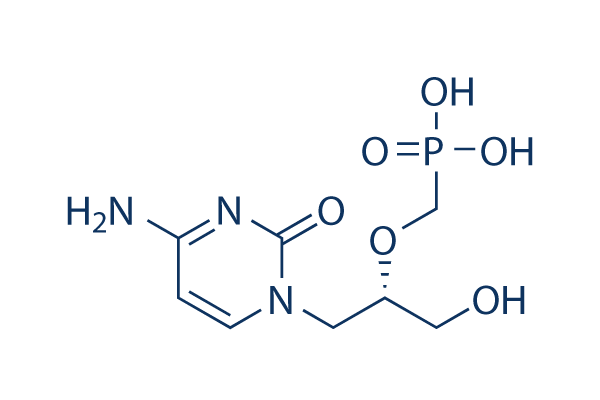
Structure chimique
Poids moléculaire: 279.19
Contrôle Qualité
| Cibles apparentées | HDAC PARP ATM/ATR DNA-PK WRN Topoisomerase PPAR Sirtuin Casein Kinase eIF |
|---|---|
| Autre DNA/RNA Synthesis Inhibiteurs | CX-5461 (Pidnarulex) B02 SCR7 Favipiravir (T-705) EED226 RK-33 BMH-21 Triapine (3-AP) Carmofur YK-4-279 |
Culture cellulaire, traitement et concentration de travail
| Lignées cellulaires | Type dessai | Concentration | Temps dincubation | Formulation | Description de lactivité | PMID |
|---|---|---|---|---|---|---|
| HEL cells | Function assay | Compound was tested for anti-viral activity against HSV-1(KOS) in HEL cells, EC50=0.57 μM | ||||
| MRC-5 cells | Function assay | Inhibitory activity against cytopathic effect of HSV-2(E 194) in MRC-5 cells, IC50=10 μM | ||||
| NHDF cells | Function assay | Inhibitory activity against replication of HCMV in NHDF cells, IC50=0.5 μM | ||||
| HFF cells | Function assay | Antiviral activity against Vaccinia virus Copenhagen in HFF cells assessed as reduction in cytopathogenicity, EC50=3.2 μM | ||||
| HFF cells | Function assay | Antiviral activity against Cowpox virus Brighton in HFF cells assessed as reduction in cytopathogenicity, EC50=7.1 μM | ||||
| HFF cells | Function assay | Antiviral activity against vaccinia virus Copenhagen measured as cytopathogenicity in HFF cells, EC50=6.9 μM | ||||
| bone marrow cells | Cytotoxicity assay | Cytotoxicity against human bone marrow cells assessed as inhibition of colony forming unit of granulocyte/macrophage, IC50=10 μM | ||||
| HFF cells | Function assay | Antiviral activity against Human CMV T2241 in HFF cells by SEAP assay, IC50=0.3 μM | ||||
| MRC5 cells | Function assay | Antiviral activity against Human CMV Towne in MRC5 cells by PRA, IC50=0.3 μM | ||||
| UC1B cells | Function assay | Antiviral activity against Murine polyomavirus MN/RDE Toronto in mouse UC1B cells assessed as reduction of virus-induced cytopathogenicity, EC50=13 μM | ||||
| african green monkey Vero cells | Function assay | Antiviral activity against Herpes simplex virus 1 F infected in african green monkey Vero cells assessed as plaque reduction after 36 to 48 hrs, EC50=14.4 μM | ||||
| HEL cells | Function assay | 3 days | Antiviral activity against HCMV AD169 infected in HEL cells assessed as reduction of virus-induced cytopathogenicity after 3 days, EC50=0.41 μM | |||
| HEL cells | Function assay | 3 days | Antiviral activity against HCMV Davis infected in HEL cells assessed as reduction of virus-induced cytopathogenicity after 3 days, EC50=0.41 μM | |||
| HFF cells | Function assay | Antiviral activity against Cytomegalovirus CMV T2211 infected in HFF cells by SEAP reporter gene assay, EC50=0.22 μM | ||||
| HEL cells | Function assay | Antiviral activity against ganciclovir-resistant HCMV AD169 clone 4 infected in HEL cells assessed as inhibition of virus-induced cytopathicity, EC50=0.74 μM | ||||
| HEL cells | Function assay | Antiviral activity against HCMV Davis infected in human HEL cells assessed inhibition of virus-induced cytopathicity after 7 days postinfection, EC50=0.5 μM | ||||
| HEL cells | Function assay | Antiviral activity against HCMV AD169 infected in human HEL cells assessed inhibition of virus-induced cytopathicity after 7 days postinfection, EC50=0.3 μM | ||||
| HEL cells | Function assay | Antiviral activity against foscarnet-resistant HCMV AD169 clone C infected in HEL cells assessed as inhibition of virus-induced cytopathicity, IC50=0.045 μM | ||||
| HFF | Proliferation assay | 3 days | Antiproliferative activity against HFF after 3 days by coulter counter assay, EC50=1.9 μM | |||
| HeLaS3 cells | Function assay | 3-5 days | Antiviral activity against Vaccinia virus IHD-J ATCC VR-156 infected in HeLaS3 cells after 3 to 5 days by plaque assay, EC50=18.74 μM | |||
| HSB2 cells | Function assay | 7 days | Antiviral activity against Human herpesvirus 6 GS infected in human HSB2 cells assessed as decrease in viral DNA accumulation after 7 days, EC50=2.7 μM | |||
| A549 cells | Function assay | Antiviral activity against Human adenovirus type 11p slobitski infected in A549 cells assessed as inhibition of DNA replication by QPCR assay, EC50=16.5 μM | ||||
| HFF cells | Function assay | Antiviral activity against Cowpox virus (Brighton Red) infected in human HFF cells assessed as reduction in viral-induced cytopathic effect by neutral red uptake assay, EC50=6.7 μM | ||||
| Cliquez pour voir plus de données expérimentales sur la lignée cellulaire | ||||||
Informations chimiques, stockage et stabilité
| Poids moléculaire | 279.19 | Formule | C8H14N3O6P |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 113852-37-2 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | HPMPC, GS 0504 | Smiles | C1=CN(C(=O)N=C1N)CC(CO)OCP(=O)(O)O | ||
Solubilité
|
In vitro |
Water : 3 mg/mL
DMSO
: Insoluble
Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| In vitro |
Cidofovir inhibe l'infection par le cytomégalovirus humain (HCMV) dans les cellules cultivées. Ce composé inhibe la formation de plaques de CMV même lorsqu'il est ajouté aux cellules 48 heures après l'infection avec une IC50 de 0,9 μg/mL pour Davis et de 1,6 μg/mL pour les souches AD-169, respectivement. Il inhibe également l'infection par le virus de l'herpès simplex. De plus, ce produit chimique bloque la fusion cellulaire induite par le HSV-1 dans les cellules rénales de singe et bloque l'expression des protéines spécifiques du HSV-1 et la synthèse de l'ADN viral. |
|---|---|
| In vivo |
Cidofovir (5 mg/kg/jour) par voie sous-cutanée pendant 5 jours réduit significativement le titre d'infectivité virale moyen dans le sang, la rate, les poumons et les glandes salivaires chez les cobayes infectés. Ce composé réduit significativement la lymphocytose et l'indice tissulaire moyen de la rate chez les animaux infectés. . Il supprime toutes les manifestations (lésions cutanées, paralysie des pattes arrière et mortalité) chez les souris nues infectées par voie intracutanée avec le HSV-1 ou le HSV-2. La caractéristique la plus remarquable de ce composé est qu'une seule administration du composé, même 4 jours après l'infection, confère une protection significative contre l'infection par le HSV-1 ou le HSV-2. Ce produit chimique inhibe la croissance de la tumeur mélanomateuse très agressive provenant des cellules de mélanome B16 de souris greffées par voie sous-cutanée chez des souris C57Bl6/J. |
Références |
|
Informations sur lessai clinique
(données du https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Promoteur/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT04542252 | Completed | Drug Drug Interaction |
SymBio Pharmaceuticals |
November 9 2020 | Phase 1 |
| NCT01610765 | Withdrawn | Herpes Simplex Virus |
University of Alabama at Birmingham |
January 2016 | Phase 1|Phase 2 |
| NCT01816646 | Completed | Blood And Marrow Transplantation |
M.D. Anderson Cancer Center|Gilead Sciences |
September 2013 | Phase 1 |
| NCT00780182 | Completed | Healthy |
Chimerix|National Institutes of Health (NIH) |
October 2008 | Phase 1 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
