pour la recherche uniquement
PluriSIn #1 (NSC 14613) SCD inhibiteur
Réf. CatalogueS8076
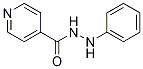
Structure chimique
Poids moléculaire: 213.24
Contrôle Qualité
- Cité dans Nature Medicine pour sa qualité supérieure
- COA
- NMR
- HPLC
- SDS
- Fiche technique
| Cibles apparentées | Dehydrogenase HSP Transferase P450 (e.g. CYP17) PDE phosphatase PPAR Vitamin Carbohydrate Metabolism Mitochondrial Metabolism |
|---|---|
| Autre SCD Inhibiteurs | MK-8245 A939572 MF-438 CVT-11127 Aramchol CAY10566 |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 213.24 | Formule | C12H11N3O |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 91396-88-2 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | N/A | Smiles | C1=CC=C(C=C1)NNC(=O)C2=CC=NC=C2 | ||
Solubilité
|
In vitro |
DMSO
: 43 mg/mL
(201.65 mM)
Water : Insoluble Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
SCD1
|
|---|---|
| In vitro |
PluriSIn #1 (NSC 14613) a un effet cytotoxique robuste, rapide et sélectif envers les hPSCs, l'apoptose étant le mécanisme central de mort cellulaire qu'il active. Ce composé entraîne un stress du RE dans les hPSCs, induisant une diminution d'environ 30 % de la synthèse protéique à 20 μM. Il provoque également une diminution d'environ 65 % de l'activité de la stéaroyl-CoA désaturase (SCD1) et empêche la formation de tératomes à partir de hPSCs non différenciées. PluriSIns inhibe également les mPSCs et entrave le développement embryonnaire de la souris.
|
| Essai kinase |
Essais d'activité SCD1
|
|
Les cellules sont ensemencées dans des plaques à 6 puits à une densité de 50 000 à 100 000 cellules par puits. 24 h plus tard, 20 μM de PluriSIn #1 (NSC 14613) ou 0,2 % de DMSO-contrôle sont ajoutés aux cellules. Après 12 h d'incubation à 37 ℃, 5 % de CO2, l'ancien milieu est retiré, les cellules sont lavées avec du PBS et un nouveau milieu contenant 2,3 μM de 0,75 UCi [1-14C] d'acide stéarique est ajouté. Les cellules sont incubées pendant 4 h maximum à 37 ℃, 5 % de CO2. Après la période d'incubation, le milieu est jeté et les cellules sont lavées 3 fois avec 2 mL de PBS. 2 mL du mélange n-hexane: isopropanol (3:2 v:v) sont ajoutés, et les cellules sont incubées pendant 30 min à 37 ℃, 5 % de CO2. 2 mL de solution de Folch (chloroforme: méthanol, 2:1, v:v) sont ensuite ajoutés. Le liquide est transféré dans des tubes pour la séparation de phase en ajoutant 1 mL d'eau. La phase organique inférieure est évaporée et utilisée pour la saponification des lipides et la séparation par CCM de l'acide stéarique [1-14C] libre (substrat) et de l'acide oléique [1-14C] (produit formé). Les lipides extraits des cellules sont appliqués sur des plaques de CCM préalablement immergées dans 10 % de NO3 Ag et activées à 120℃x60 min. De l'acide stéarique et oléique non marqué est ajouté à chaque point d'application comme porteurs et comme étalons internes pour l'identification. Les plaques sont développées avec un mélange de solvants Chloroforme:MeOH:AcH:DDW (90:8:1:0.8). Les acides gras libres sont détectés par U.V. après pulvérisation de la CCM avec une solution de 2',7',dichlorofluorescéine. Les taches correspondant à l'acide stéarique et oléique sont grattées et la radioactivité est comptée dans un compteur à scintillation. L'activité de la désaturase SCD1 est calculée à partir du pourcentage de conversion du substrat en produit et de la conversion en pmol/min/106 cellules.
|
Références |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
