pour la recherche uniquement
E7080 (Lenvatinib) VEGFR inhibiteur
Réf. CatalogueS1164
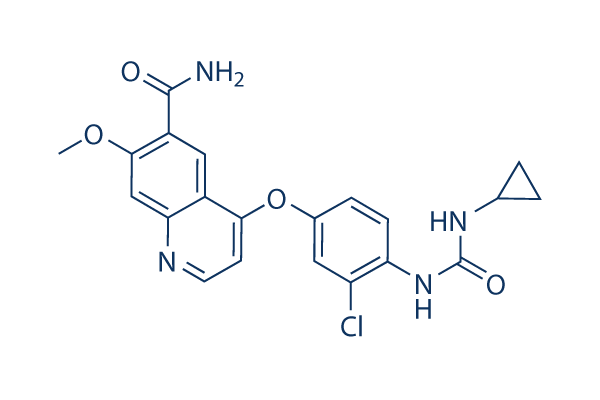
Structure chimique
Poids moléculaire: 426.85
Contrôle Qualité
Produits souvent utilisés avec E7080 (Lenvatinib)
| Cibles apparentées | EGFR PDGFR FGFR c-Met Src MEK CSF-1R FLT3 HER2 c-Kit |
|---|---|
| Autre VEGFR Inhibiteurs | SAR131675 SU 5402 Cediranib (AZD2171) Vatalanib (PTK787) 2HCl Anlotinib (AL3818) Dihydrochloride Linifanib (ABT-869) Apatinib (YN968D1) Apatinib (YN968D1) mesylate Ki8751 ZM 323881 HCl |
Culture cellulaire, traitement et concentration de travail
| Lignées cellulaires | Type dessai | Concentration | Temps dincubation | Formulation | Description de lactivité | PMID |
|---|---|---|---|---|---|---|
| TPC-1 and K1 cells | Function assay | 50 μM | 24 h | The inhibitory effects of lenvatinib on the viability of both cell lines were not influenced by the leptin treatment. | 30906321 | |
| ATC cells | Function assay | 1, 25 and 50 μM | 72 h | Phosphorylated/non-phosphorylated Akt or ERK1/2 proteins (evaluated by ELISA) in lenvatinib-treated samples were significantly reduced in ATC cell cultures. | 29517103 | |
| HCC cell lines Hep3B2.1-7, HuH-7, and JHH-7 | Proliferation assay | 6 days | Lenvatinib showed selective and potent antiproliferative activity against the HCC cell lines Hep3B2.1‐7, HuH‐7, and JHH‐7, with IC50 values of 0.23, 0.42, and 0.64 μmol/L, respectively. | 29733511 | ||
| HT29 cells | Cytotoxicity assay | 25, 50 nM | 72 h | cytotoxic dose: 50 nM and noncytotoxic dose: 25 nM | 24815456 | |
| DX3 and U2OS cells | Function assay | 1 μM and 10 μM | 16 hours | Lenvatinib inhibit tumor cells migration and invasion at concentrations that both inhibit its known targets and are achievable clinically. | 21781317 | |
| Cliquez pour voir plus de données expérimentales sur la lignée cellulaire | ||||||
Informations chimiques, stockage et stabilité
| Poids moléculaire | 426.85 | Formule | C21H19ClN4O4 |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 417716-92-8 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | E7080 | Smiles | COC1=CC2=NC=CC(=C2C=C1C(=O)N)OC3=CC(=C(C=C3)NC(=O)NC4CC4)Cl | ||
Solubilité
|
In vitro |
DMSO
: 20 mg/mL
(46.85 mM)
Water : Insoluble Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
RET
VEGFR2/KDR
(Cell-free assay) 4.0 nM
VEGFR3/FLT4
(Cell-free assay) 5.2 nM
VEGFR1/FLT1
(Cell-free assay) 22 nM
PDGFRβ
(Cell-free assay) 39 nM
FGFR1
(Cell-free assay) 46 nM
PDGFRα
(Cell-free assay) 51 nM
Kit
(Cell-free assay) 100 nM
|
|---|---|
| In vitro |
E7080, en tant qu'inhibiteur puissant de l'angiogenèse in vitro, montre un effet inhibiteur significatif sur la signalisation VEGF/KDR et SCF/Kit. Selon les tests de tyrosine kinase et de sérine/thréonine kinase in vitro, ce composé inhibe Flt-1, KDR, Flt-4 avec une IC50 de 22, 4,0 et 5,2 nM, respectivement. En plus de ces kinases, ce composé inhibe également les Protein Tyrosine Kinase FGFR1 et PDGFR avec des valeurs d'IC50 de 46, 51 et 100 nM pour FGFR1, PDGFRα et PDGFRβ, respectivement. Ce composé inhibe puissamment la phosphorylation de VEGFR2 (IC50, 0,83 nM) et VEGFR3 (IC50, 0,36 nM) dans les HUVEC qui est stimulée par le VEGF et le VEGF-C, respectivement. Une étude récente montre que le traitement par ce composé (à 1 μM et 10 μM) entraîne une inhibition significative de la migration et de l'invasion cellulaire en inhibant la signalisation FGFR et PDGFR. |
| Essai kinase |
Essai kinase in vitro
|
|
Les essais de Protein Tyrosine Kinase sont réalisés par HTRF (KDR, VEGFR1, FGFR1, c-Met, EGFR) et ELISA (PDGFRβ), en utilisant les domaines kinase recombinants des récepteurs. Dans les deux essais, 4 μL de dilutions en série de ce composé sont mélangés dans une plaque à 96 puits à fond rond avec 10 μL d'enzyme, 16 μL de solution de poly (GT) (250 ng) et 10 μL de solution d'ATP (1 μM ATP) (la concentration finale de DMSO est de 0,1%). Dans les puits pour les blancs, aucune enzyme n'est ajoutée. Dans les puits de contrôle, aucun article testé n'est ajouté. La réaction de la kinase est initiée en ajoutant une solution d'ATP à chaque puits. Après 30 minutes d'incubation à 30°C, la réaction est arrêtée par l'ajout de 0,5 M d'EDTA (10 μL/puits) au mélange réactionnel dans chaque puits. Un tampon de dilution adéquat à chaque essai kinase est ajouté au mélange réactionnel. Dans l'essai HTRF, 50 μL du mélange réactionnel sont transférés dans une plaque EIA/RIA noire à 96 puits et 1/2 surface, une solution HTRF (50 μL/puits) est ajoutée au mélange réactionnel, puis l'activité kinase est déterminée par mesure de la fluorescence avec un détecteur de fluorescence résolu en temps à une longueur d'onde d'excitation de 337 nm et des longueurs d'onde d'émission de 620 et 665 nm. Dans l'ELISA, 50 μL du mélange réactionnel sont incubés dans des plaques de polystyrène à 96 puits revêtues d'avidine à température ambiante pendant 30 minutes. Après lavage avec le tampon de lavage, une solution de PY20-HRP (70 μL/puits) est ajoutée et le mélange réactionnel est incubé à température ambiante pendant 30 minutes. Après lavage avec le tampon de lavage, un réactif TMB (100 μL/puits) est ajouté à chaque puits. Après plusieurs minutes (10 à 30 minutes), 1 M H3PO4 (100 μL/puits) est ajouté à chaque puits. L'activité kinase est déterminée par mesure de l'absorbance à 450 nm avec un lecteur de microplaques.
|
|
| In vivo |
Lorsqu'il est administré par voie orale dans un modèle de xénogreffe H146, le Lenvatinib (E7080) inhibe la croissance de la tumeur H146 à 30 et 100 mg/kg de manière dose-dépendante et entraîne une régression tumorale à 100 mg/kg. De plus, ce composé à 100 mg/kg diminue la densité des microvaisseaux plus que le traitement par anticorps anti-VEGF et imatinib. Il inhibe significativement la croissance tumorale locale dans un modèle de coussinet adipeux mammaire (m.f.p.) MDA-MB-231 avec des RTV (volume tumoral calculé au jour 8/volume tumoral au jour 1) de 0,81, et réduit à la fois l'angiogenèse et la lymphangiogenèse des nodules métastatiques établis de la tumeur MDA-MB-231 dans les ganglions lymphatiques. |
Références |
|
Applications
| Méthodes | Biomarqueurs | Images | PMID |
|---|---|---|---|
| Western blot | Vimentin / E-cadherin / Snail / Zeb1 β-catenin Ki-67 / Cyclin D1 / CDK4 / p21 / p53 / Apaf-1 / p-NFκB / Bcl-2 / Cleaved-caspase 3 phospho-RET phospho-FGFR1 / FGFR1 /phospho-FRS2 / FRS2 / phospho-MEK / phospho-ERK |
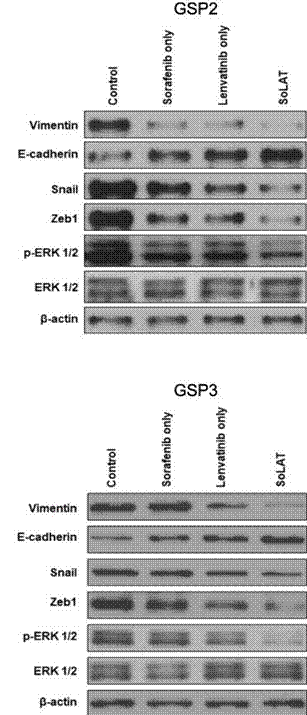
|
30286728 |
| Growth inhibition assay | Cell viability |
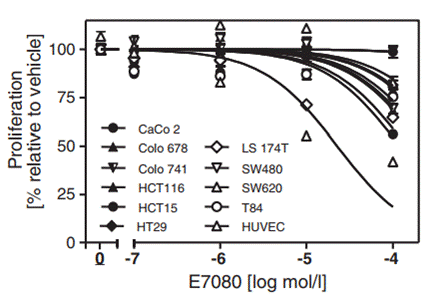
|
25425971 |
Informations sur lessai clinique
(données du https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Promoteur/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT06161558 | Not yet recruiting | Neoplasms |
National Cancer Institute (NCI)|National Institutes of Health Clinical Center (CC) |
May 15 2024 | Phase 1 |
| NCT05846724 | Not yet recruiting | Kaposi Sarcoma|Classic Kaposi Sarcoma|Refractory Kaposi Sarcoma |
Fondazione IRCCS Ca'' Granda Ospedale Maggiore Policlinico |
February 1 2024 | Phase 2 |
| NCT05903833 | Not yet recruiting | Recurrent Vulvar Cancer|Persistent Vulvar Cancer|Metastatic Vulva Cancer|Locally Advanced Vulvar Cancer |
AGO Research GmbH |
January 1 2024 | Phase 2 |
| NCT05901194 | Not yet recruiting | Hepatocellular Carcinoma Non-resectable |
Assistance Publique - Hôpitaux de Paris|Laboratoire EISAI |
June 2023 | Phase 1|Phase 2 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
