pour la recherche uniquement
Pilaralisib (XL147) PI3K inhibiteur
Réf. CatalogueS7645
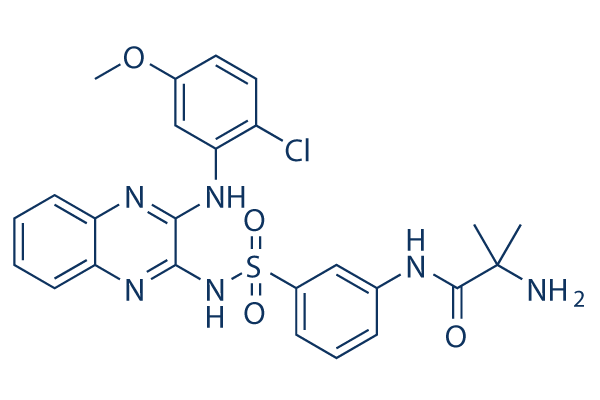
Structure chimique
Poids moléculaire: 541.02
Contrôle Qualité
- Cité dans Nature Medicine pour sa qualité supérieure
- COA
- NMR
- SDS
- Fiche technique
| Cibles apparentées | Akt mTOR GSK-3 ATM/ATR DNA-PK AMPK PDPK1 PTEN PP2A PDK |
|---|---|
| Autre PI3K Inhibiteurs | GDC-0077 (Inavolisib) SAR405 Quercetin (Sophoretin) LY294002 XL147 analogue Tersolisib (STX-478) Buparlisib (BKM120) 740 Y-P (PDGFR 740Y-P) GO-203 TFA Eganelisib (IPI-549) |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 541.02 | Formule | C25H25ClN6O4S |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 934526-89-3 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | N/A | Smiles | CC(C)(C(=O)NC1=CC(=CC=C1)S(=O)(=O)NC2=NC3=CC=CC=C3N=C2NC4=C(C=CC(=C4)OC)Cl)N | ||
Solubilité
|
In vitro |
DMSO
: 100 mg/mL
(184.83 mM)
Water : Insoluble Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
PI3Kγ
23 nM
PI3Kβ
36 nM
PI3Kδ
36 nM
PI3Kα
39 nM
|
|---|---|
| In vitro |
Dans les lignées cellulaires du Pediatric Preclinical Testing Program (PPTP), le Pilaralisib (XL147) présente une activité cytotoxique, avec une valeur d'IC50 relative médiane de 10,9 mM (plage de 2,7 mM à 24,5 mM).
|
| Essai kinase |
Tests d'inhibition de la kinase in vitro
|
|
L'activité kinase pour les isoformes de PI3K est mesurée comme le pourcentage d'ATP consommé après la réaction kinase en utilisant la chimioluminescence couplée luciférase-luciférine, avec des concentrations d'ATP approximativement égales au Km pour chaque kinase respective. Les réactions kinase sont initiées en combinant les composés testés, l'ATP et la kinase dans un volume de 20 μL. Les concentrations finales d'enzymes PI3Kα, PI3Kβ, PI3Kγ et PI3Kδ sont respectivement de 0,5, 8, 20 et 2 nM. Il est à noter que 0,5 μL de diméthylsulfoxyde (DMSO) contenant diverses concentrations de ce composé est mélangé avec 10 μL de solution enzymatique (2×concentration). Les réactions kinase sont initiées par l'ajout de 10 μL de phosphatidylinositol hépatique et de solution d'ATP (2×concentration). Les concentrations d'essai pour VPS34, ATP et phosphatidylinositol sont respectivement de 40 nM, 1 μM et 5 μM.
|
|
| In vivo |
Chez des souris BALB/c nu/nu, le Pilaralisib (XL147) (100 mg/kg, p.o.) induit une inhibition de la croissance tumorale pour les xénogreffes de gliome solide et est bien toléré, avec seulement 0,7% de taux de toxicité dans les groupes traités, similaire à celui observé chez les animaux témoins. Chez la souris femelle athymique, il (100 mg/kg, p.o.) retarde significativement la croissance tumorale sans toxicité significative liée au médicament.
|
Références |
|
Applications
| Méthodes | Biomarqueurs | Images | PMID |
|---|---|---|---|
| Western blot | IGF-1R / AKT / MAPK |
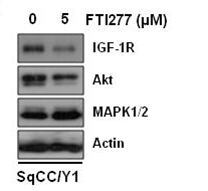
|
22113431 |
| Immunofluorescence | PAK phospho-PAK |
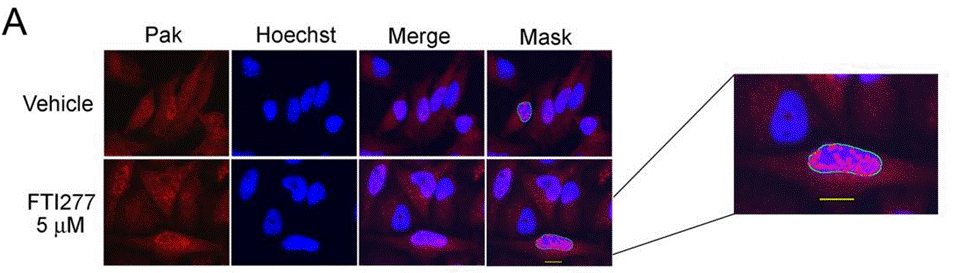
|
23915247 |
Informations sur lessai clinique
(données du https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Promoteur/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT01240460 | Completed | Glioblastoma|Astrocytoma Grade IV |
Sanofi |
January 2011 | Phase 1 |
| NCT01013324 | Completed | Endometrial Cancer|Endometrial Neoplasms |
Sanofi |
January 2010 | Phase 2 |
| NCT00756847 | Completed | Cancer|Non-Small Cell Lung Cancer|Endometrial Carcinoma|Ovarian Carcinoma |
Sanofi |
September 2008 | Phase 1 |
| NCT00704392 | Withdrawn | Cancer|Non-small-cell Lung Cancer|Breast Cancer |
Exelixis |
June 2008 | Phase 1 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
