pour la recherche uniquement
Gedatolisib (PKI-587) PI3K inhibiteur
Réf. CatalogueS2628
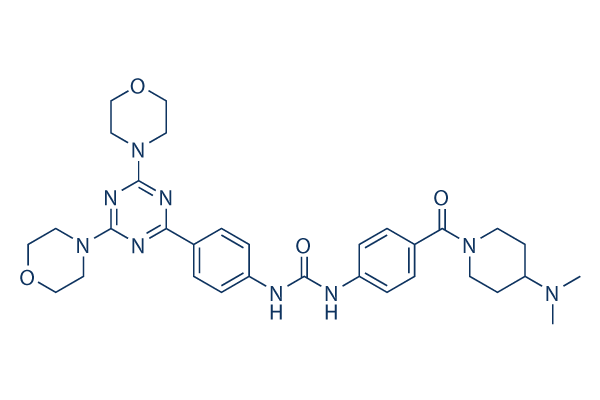
Structure chimique
Poids moléculaire: 615.73
Contrôle Qualité
| Cibles apparentées | Akt mTOR GSK-3 ATM/ATR DNA-PK AMPK PDPK1 PTEN PP2A PDK |
|---|---|
| Autre PI3K Inhibiteurs | GDC-0077 (Inavolisib) SAR405 Quercetin (Sophoretin) LY294002 XL147 analogue Tersolisib (STX-478) Buparlisib (BKM120) 740 Y-P (PDGFR 740Y-P) GO-203 TFA Eganelisib (IPI-549) |
Culture cellulaire, traitement et concentration de travail
| Lignées cellulaires | Type dessai | Concentration | Temps dincubation | Formulation | Description de lactivité | PMID |
|---|---|---|---|---|---|---|
| MDA-MB-361 cells | Cytotoxicity assay | Cytotoxicity against human MDA-MB-361 cells, IC50=0.004 μM | ||||
| PC3MM2 cells | Cytotoxicity assay | Cytotoxicity against human PC3MM2 cells, IC50=0.0131 μM | ||||
| MDA-MB-361 cells | Function assay | Inhibition of Akt T308 phosphorylation in human MDA-MB-361 cells by Western blotting, IC50=0.008 μM | ||||
| MDA-MB-361 cells | Function assay | Inhibition of Akt S473 phosphorylation in human MDA-MB-361 cells by Western blotting, IC50=0.01 μM | ||||
| MDA-MB-361 cells | Function assay | Inhibition of eNOS phosphorylation in human MDA-MB-361 cells by Western blotting | ||||
| MDA-MB-361 cells | Function assay | Inhibition of PARS40 phosphorylation in human MDA-MB-361 cells by Western blotting | ||||
| MDA-MB-361 cells | Function assay | Inhibition of GSK3 kinase phosphorylation in human MDA-MB-361 cells by Western blotting | ||||
| MDA-MB-361 cells | Function assay | Inhibition of mTOR TORC1 kinase activity in human MDA-MB-361 cells assessed as suppression of p70S6K phosphorylation at < 30 nM | ||||
| MDA-MB-361 cells | Function assay | Inhibition of mTOR TORC1 kinase activity in human MDA-MB-361 cells assessed as suppression of 4EBP1 phosphorylation at < 30 nM | ||||
| MDA-MB-361 cells | Function assay | Inhibition of Akt T308 phosphorylation in human MDA-MB-361 cells xenografted mouse model upto 36 hrs | ||||
| MDA-MB-361 cells | Function assay | Inhibition of Akt S473 phosphorylation in human MDA-MB-361 cells xenografted mouse model upto 36 hrs | ||||
| MDA-MB-361 cells | Function assay | Induction of PARP cleavage in human MDA-MB-361 cells xenografted mouse model upto 18 hrs | ||||
| MDA-MB-361 cells | Function assay | Antitumor activity against human MDA-MB-361 cells xenografted mouse model assessed as reduction in tumor volume at 20 mg/kg, iv on day 1, 5, 9 | ||||
| SF9 insect cells | Function assay | 2 h | Inhibition of human PI3Kalpha expressed in SF9 insect cells after 2 hrs by fluorescence polarization assay, IC50=0.0004 μM | |||
| SF9 insect cells | Function assay | 2 h | Inhibition of human PI3Kgamma expressed in SF9 insect cells after 2 hrs by fluorescence polarization assay, IC50=0.011μM | |||
| MDA-MB-361 cells | Growth inhibition assay | 72 h | Growth inhibition of human MDA-MB-361 cells after 72 hrs, IC50=0.003 μM | |||
| human PC3 cells | Growth inhibition assay | 72 h | Growth inhibition of human PC3 cells after 72 hrs, IC50=0.011 μM | |||
| Cliquez pour voir plus de données expérimentales sur la lignée cellulaire | ||||||
Informations chimiques, stockage et stabilité
| Poids moléculaire | 615.73 | Formule | C32H41N9O4 |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 1197160-78-3 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | PF-05212384 | Smiles | CN(C)C1CCN(CC1)C(=O)C2=CC=C(C=C2)NC(=O)NC3=CC=C(C=C3)C4=NC(=NC(=N4)N5CCOCC5)N6CCOCC6 | ||
Solubilité
|
In vitro |
DMSO
: 3 mg/mL
(4.87 mM)
Ethanol : 1 mg/mL Water : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
PI3Kα
(Cell-free assay) 0.4 nM
mTOR
(Cell-free assay) 1.6 nM
PI3Kγ
(Cell-free assay) 5.4 nM
|
|---|---|
| In vitro |
Gedatolisib (PKI-587) montre une activité inhibitrice puissante contre PI3K-α, PI3K-γ et mTOR avec des IC50 de 0,4 nM, 5,4 nM et 1,6 nM, respectivement. De plus, il présente également sa puissance contre les formes mutantes les plus fréquemment rencontrées de PI3Kα, notamment le H1047R et le E545K avec des IC50 de 0,6 nM et 0,6 nM, respectivement. Corrélié avec la suppression de la phosphorylation des protéines de la voie de signalisation PI3K/mTOR, ce composé provoque une inhibition de la croissance des cellules tumorales dans les lignées cellulaires MDA-361 et PC3-MM2 avec des IC50 de 4 nM et 13,1 nM, respectivement.
|
| Essai kinase |
Test de la kinase PI3K et mTOR
|
|
Les tests enzymatiques sont réalisés en format de polarisation de fluorescence (FP), adapté du protocole du kit d'essai PI3K FP Echelon K-1100. Les PI3K de classe I humaines et les mutants de PI3K-α (E545K et H1047R) sont produits dans Sf9 ou achetés chez Upstate Biotech. Le GST-GRP1 (murin) est produit dans Escherichia coli et isolé par GST-Sepharose. Les tampons d'essai sont le tampon de réaction [20 mM HEPES (pH 7,1), 2 mM MgCl2, 0,05 % CHAPS et 0,01 % β-mercaptoéthanol] et le tampon d'arrêt/détection [100 mM HEPES (pH 7,5), 4 mM EDTA, 0,05 % CHAPS]. La réaction FP est réalisée pendant 30 minutes à température ambiante dans 20 μL de tampon de réaction contenant 20 μM de phosphatidylinositol 4,5-bisphosphate (PIP2), 25 μM d'ATP et <4 % de DMSO. La réaction FP est arrêtée avec 20 μL de tampon d'arrêt/détection (sonde de 10 nM et GST-GRP de 40 nM), et après 2 heures, les données sont collectées à l'aide d'un lecteur de plaques Envision. Les tests de routine avec FLAG-TOR purifié (FL et 3.5) sont effectués dans des plaques à 96 puits comme suit. Les enzymes sont d'abord diluées dans le tampon d'essai de kinase (10 mM Hepes (pH 7,4), 50 mM NaCl, 50 mM β-glycérophosphate, 10 mM MnCl2, 0,5 mM DTT, 0,25 μM microcystine LR et 100 μg/mL de BSA). Dans chaque puits, 12 μL de l'enzyme diluée sont mélangés brièvement avec 0,5 μL d'inhibiteur testé ou de véhicule témoin diméthylsulfoxyde (DMSO), où l'inhibiteur testé est Gedatolisib (PKI-587). La réaction de la kinase est initiée par l'ajout de 12,5 μL de tampon d'essai de kinase contenant de l'ATP et de l'His6-S6K pour donner un volume de réaction final de 25 μL contenant 800 ng/mL de FLAG-TOR, 100 μM d'ATP et 1,25 μM d'His6-S6K. La plaque de réaction est incubée pendant 2 heures (linéaire à 1–6 heures) à température ambiante avec une agitation douce, puis arrêtée par l'ajout de 25 μL de tampon d'arrêt (20 mM Hepes (pH 7,4), 20 mM EDTA et 20 mM EGTA).
|
|
| In vivo |
Le traitement par Gedatolisib (PKI-587) à 25 mg/kg i.v. chez des souris nues entraîne une faible clairance plasmatique (7 (mL/min)/kg), un volume de distribution élevé (7,2 L/kg) et une longue demi-vie (14,4 heures). Dans le modèle de xénogreffe MDA-361, il produit une puissante efficacité antitumorale avec la dose efficace minimale (MED) de 3 mg/kg contre les tumeurs MDA-361 et la dose unique maximale tolérée (MTD) de 30 mg/kg. Alors que dans le modèle de xénogreffe H1975 (carcinome pulmonaire non à petites cellules, EGFR muté [L858R, T790M]), ce composé à 25 mg/kg pendant 7 semaines entraîne une survie de 90 % du groupe traité.
|
Références |
|
Applications
| Méthodes | Biomarqueurs | Images | PMID |
|---|---|---|---|
| Growth inhibition assay | Cell viability |
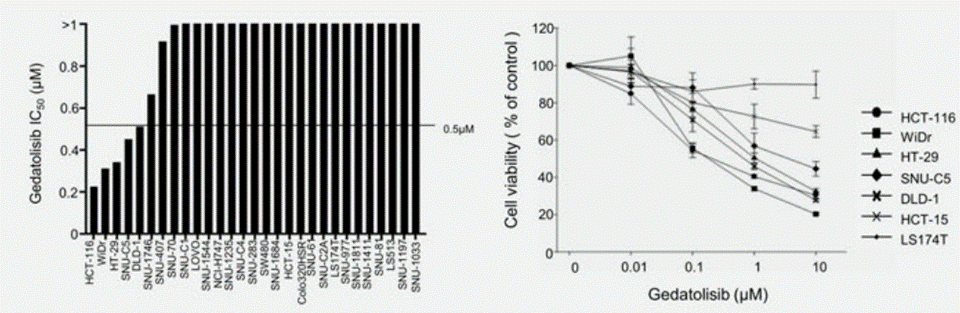
|
29978469 |
| Western blot | p-AKT / p-mTOR / p-p70S6K / p-S6K / p-4E-BP1 / AKT / mTOR / p70S6K / S6K / 4EBP1 TSC1 / TSC2 / Raptor |
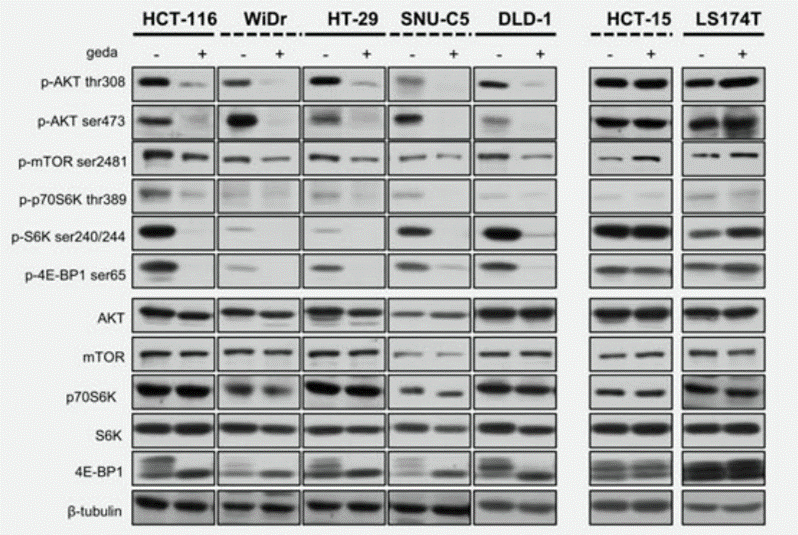
|
29978469 |
Informations sur lessai clinique
(données du https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Promoteur/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT02438761 | Terminated | Therapy-related Acute Myeloid Leukemia and Myelodysplastic Syndrome|Acute Myeloid Leukemia in Relapse|de Novo Acute Myeloid Leukemia at Diagnostic |
Institut Curie|Fondation ARC|National Cancer Institute France |
August 31 2015 | Phase 2 |
| NCT02069158 | Completed | Breast Cancer|NSCLC|Ovary Cancer|Endometrial Cancer|Small Cell Lung Cancer (SCLC)|Head and Neck (HNSCC) |
Cristiana Sessa|Oncology Institute of Southern Switzerland |
April 2014 | Phase 1 |
| NCT01420081 | Terminated | Endometrial Neoplasms |
Pfizer |
January 19 2012 | Phase 2 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
