pour la recherche uniquement
Plerixafor (AMD3100) 8HCl CXCR antagoniste
Réf. CatalogueS3013
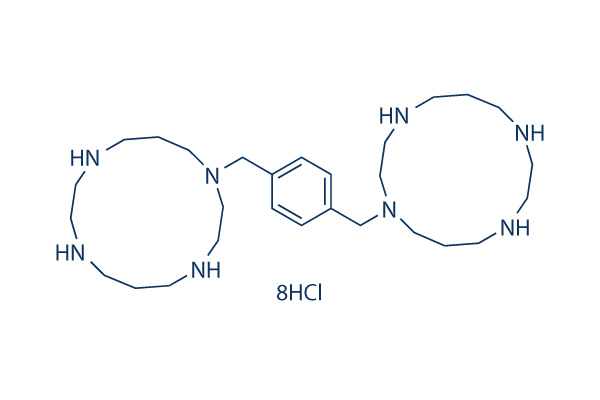
Structure chimique
Poids moléculaire: 794.47
Contrôle Qualité
| Cibles apparentées | Hedgehog/Smoothened PKA Adrenergic Receptor AChR 5-HT Receptor Histamine Receptor Dopamine Receptor Ras KRas GPR |
|---|---|
| Autre CXCR Inhibiteurs | AZD5069 SB 225002 Reparixin (Repertaxin) WZ811 Navarixin (SCH-527123) LIT-927 AMG 487 SX-682 LY2510924 Danirixin (GSK1325756) |
Culture cellulaire, traitement et concentration de travail
| Lignées cellulaires | Type dessai | Concentration | Temps dincubation | Formulation | Description de lactivité | PMID |
|---|---|---|---|---|---|---|
| CHOK1 cells | Function assay | Displacement of [125I]SDF1alpha from CXCR4 expressed in CHOK1 cells, IC50=0.81 nM | 17715128 | |||
| GHOST CXCR4 cell line | Function assay | Inhibitory concentration of compound against HIV-1 LAI strain in GHOST CXCR4 cell line, IC50=0.95 nM | 14698189 | |||
| HEK293 cells | Function assay | 2 days | Antiviral activity against T20-resistant HIV1 NL4-3 infected in HEK293 cells assessed as inhibition of viral replication after 2 days, IC50=2.3 nM | 19451305 | ||
| PBMC cells | Function assay | Effective concentration of compound against HIV-1 89.6 strain in PBMC cells, EC50=3.8 nM | 14698189 | |||
| human MT4 cells | Function assay | 4 days | Antiviral activity against HIV1 3B infected in human MT4 cells assessed as inhibition of virus replication after 4 days by MTT assay, EC50=4 nM | 20043638 | ||
| human Jurkat cells | Function assay | Antagonist activity at CXCR4 in human Jurkat cells assessed as inhibition of SDF1-induced cell migration, IC50=27.4 nM | 19188071 | |||
| MT-4 cells | Function assay | Effective concentration of compound against HIV-1 IIIB strain in MT-4 cells, EC50=65 nM | 14698189 | |||
| rat IR983F cells | Function assay | Displacement of [125I]CXCL12 from CXCR4 in rat IR983F cells, IC50=108 nM | 19053768 | |||
| CEM-SS cells | Function assay | Effective concentration of compound against HIV-1 LAI strain in CEM-SS cells, EC50=127 nM | 14698189 | |||
| human HL60 cells | Function assay | Displacement of [125I]SDF1alpha from CXCR4 in human HL60 cells, IC50=15.2 μM | 19188071 | |||
| human MOLT4 cells | Function assay | 1000 nM | Inhibition of Mab 12G5 binding to CXCR4 expressed in human MOLT4 cells at 1000 nM by FACS analysis | 19451305 | ||
| human MT2 cells | Function assay | 1 ug/mL | 4 days | Antiviral activity against HIV1 3B infected in human MT2 cells assessed as inhibition of viral p24 antigen production at 1 ug/mL after 4 days by ELISA | 21168336 | |
| human U87 cells | Function assay | 1000 nM | Antagonist activity at CXCR4 in human U87 cells assessed as inhibition of SDF1-induced modulation of cAMP production at 1000 nM by TR-FRET assay | 17958344 | ||
| MT4 | Antiviral assay | Antiviral activity against HIV1 3B assessed as reduction in cytopathic effect in MT4 cells, EC50=0.011μM | 17034122 | |||
| U87 | Function assay | 15 mins | Antagonist activity at human CXCR4 expressed in human U87 cells expressing CD4 assessed as inhibition of CXCL12-induced cAMP production pretreated for 15 mins before forskolin challenge by TR-FRET analysis, IC50=0.695μM | 21105715 | ||
| MT4 | Antiviral assay | Antiviral activity against X4-tropic HIV1 NL4.3 infected in human MT4 cells assessed as protection from virus-induced cytopathogenicity, EC50=0.062μM | 22579418 | |||
| MT4 | Antiviral assay | 5 days | Antiviral activity against HIV1 infected in MT4 cells expressing CXCR4 assessed as inhibition of virus-induced cytopathic effect after 5 days, EC50=0.002μM | 22909088 | ||
| CHO | Function assay | Binding affinity to human recombinant CXCR4 expressed in CHO cells, Kb=0.077μM | 22909088 | |||
| CHO | Function assay | Antagonist activity at human recombinant CXCR4 expressed in CHO cells assessed as inhibition of SDF1a-induced electrical impedance by dielectric spectroscopic analysis, IC50=0.26μM | 22909088 | |||
| CD44null | Function assay | 7 days | Effect on human GBM2 cell differentiation assessed as increase in CD44null cells after 7 days by flow cytometric analysis | 22909088 | ||
| CD44null | Function assay | 7 days | Effect on human GBM1 cell differentiation assessed as increase in CD44null cells after 7 days by flow cytometric analysis | 22909088 | ||
| Cliquez pour voir plus de données expérimentales sur la lignée cellulaire | ||||||
Informations chimiques, stockage et stabilité
| Poids moléculaire | 794.47 | Formule | C28H54N8.8HCl |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 155148-31-5 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | JM 3100 8HCl,Plerixafor Octahydrochloride,AMD3100 octahydrochloride,SID791 octahydrochloride | Smiles | C1CNCCNCCCN(CCNC1)CC2=CC=C(C=C2)CN3CCCNCCNCCCNCC3.Cl.Cl.Cl.Cl.Cl.Cl.Cl.Cl | ||
Solubilité
|
In vitro |
Water : 100 mg/mL
DMSO
: Insoluble
Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
CXCL12
(Cell-free assay) 5.7 nM
CXCR4
(Cell-free assay) 44 nM
|
|---|---|
| In vitro |
Plerixafor inhibe la chimiotaxie médiatisée par CXCL12 avec une puissance légèrement supérieure à son affinité pour CXCR4. Plerixafor antagonise également la liaison du ligand SDF-1/CXCL12 avec un IC50 de 651 nM. Plerixafor inhibe la liaison GTP médiatisée par SDF-1, le flux de calcium médiatisé par SDF-1 et la chimiotaxie stimulée par SDF-1 avec des IC50 de 27 nM, 572 nM et 51 nM, respectivement. Plerixafor n'inhibe pas le flux de calcium contre les cellules exprimant CXCR3, CCR1, CCR2b, CCR4, CCR5 ou CCR7 lorsqu'elles sont stimulées avec leurs ligands cognats, et Plerixafor n'inhibe pas non plus la liaison du récepteur de LTB4. Plerixafor n'induit pas, à lui seul, un flux de calcium dans les cellules CCRF–CEM, qui expriment plusieurs GPCRs, y compris CXCR4, CCR4 et CCR7. |
| In vivo |
Une seule application topique de Plerixafor favorise la cicatrisation des plaies chez les souris diabétiques en augmentant la production de cytokines, en mobilisant les EPC de la moelle osseuse et en améliorant l'activité des fibroblastes et des monocytes/macrophages, augmentant ainsi à la fois l'angiogenèse et la vasculogenèse. Des cohortes de souris sont administrées avec du PBS, de l'IGF1, du PDGF, du SCF ou du VEGF pendant cinq jours consécutifs et du Plerixafor le 5ème jour. Le nombre et la taille des colonies sont les plus élevés chez les souris injectées avec de l'IGF1 plus Plerixafor par rapport aux groupes traités avec du PDGF, du SCF et du VEGF, en combinaison avec du Plerixafor. |
Références |
|
Applications
| Méthodes | Biomarqueurs | Images | PMID |
|---|---|---|---|
| Immunofluorescence | CXCR4 β-arrestin2 |
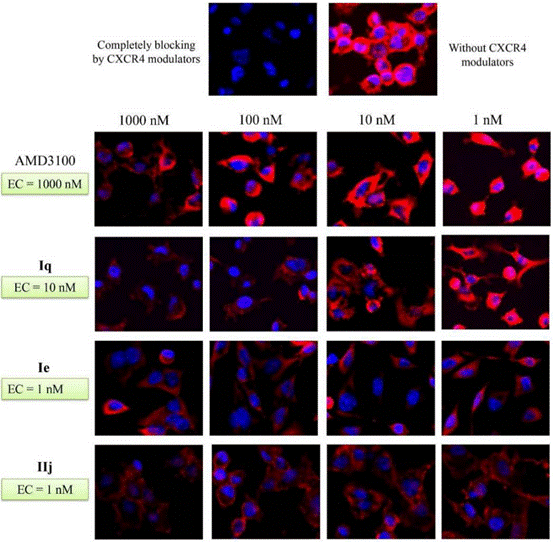
|
28521261 |
Informations sur lessai clinique
(données du https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Promoteur/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT05421416 | Not yet recruiting | Stem Cell Transplant Complications |
AHS Cancer Control Alberta |
April 1 2024 | Phase 2 |
| NCT05343572 | Recruiting | Asherman Syndrome|Atrophic Endometrium|Recurrent Implantation Failure |
Hugh Taylor|Yale University |
November 1 2023 | Early Phase 1 |
| NCT05844527 | Recruiting | Wound of Skin|Abdominal Wound |
MedRegen LLC |
November 20 2023 | Phase 2 |
| NCT05411575 | Withdrawn | COVID-19 Acute Respiratory Distress Syndrome|COVID-19 |
4Living Biotech|4P-Pharma |
July 19 2022 | Phase 2 |
| NCT05445128 | Terminated | Sickle Cell Disease |
Ensoma|bluebird bio |
June 24 2022 | Phase 2 |
| NCT05835726 | Recruiting | Multiple Myeloma|Daratumumab|Autologous Stem Cell Transplantation|Leukapheresis |
Fondazione Policlinico Universitario Agostino Gemelli IRCCS |
January 1 2022 | -- |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
