pour la recherche uniquement
β-thujaplicin DNA Methyltransferase inhibiteur
Réf. CatalogueS4771
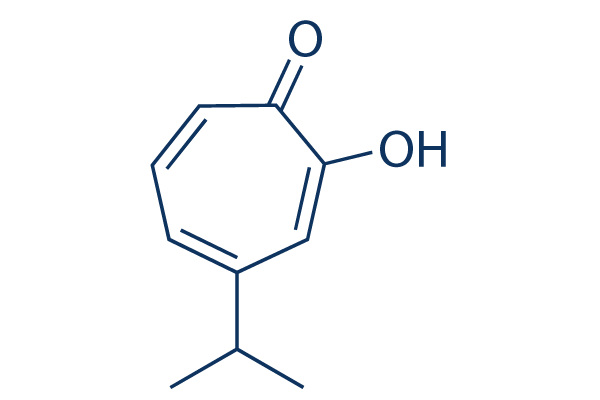
Structure chimique
Poids moléculaire: 164.20
Contrôle Qualité
| Cibles apparentées | HDAC JAK BET Histone Methyltransferase PKC PARP HIF PRMT EZH2 AMPK |
|---|---|
| Autre DNA Methyltransferase Inhibiteurs | RG108 SGI-1027 Zebularine (NSC 309132) GSK3685032 Gamma-Oryzanol CM272 Bobcat339 DC-05 2'-Deoxy-5-Fluorocytidine GSK-3484862 |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 164.20 | Formule | C10H12O2 |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 499-44-5 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | Hinokitiol, 4-Isopropyltropolone | Smiles | CC(C)C1=CC(=O)C(=CC=C1)O | ||
Solubilité
|
In vitro |
DMSO
: 32 mg/mL
(194.88 mM)
|
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| In vitro |
Dans les cellules cancéreuses du poumon, l'hinokitiol inhibe la prolifération cellulaire en induisant la réponse aux dommages de l'DNA indépendante de p53, l'autophagie (pas l'apoptose), l'arrêt du cycle cellulaire en phase S et la sénescence. L'hinokitiol induit l'autophagie dans les cellules d'adénocarcinome pulmonaire mais pas dans les fibroblastes stromaux pulmonaires humains. Il induit la sénescence cellulaire à la fois dans les cellules cancéreuses du poumon humain et les fibroblastes stromaux pulmonaires. Le traitement à l'hinokitiol révèle une inhibition concentration-dépendante de la migration des cellules de mélanome B16-F10. Il semble atteindre cet effet en réduisant l'expression de MMP-1 et en supprimant la phosphorylation des molécules de signalisation de la protéine kinase activée par les mitogènes (MAPK) telles que la kinase régulée par le signal extracellulaire (ERK) 1/2, p38 MAPK et les c-Jun N-terminal kinases (JNK). D'autre part, le traitement à l'hinokitiol inverse la dégradation de l'IκB-α et inhibe la phosphorylation du facteur nucléaire kappa B (NF-κB) p65 et de cJun dans les cellules B16-F10. De plus, l'hinokitiol supprime la translocation de p65 NF-κB du cytosol vers le noyau, suggérant une réduction de l'activation de NF-κB.
|
|---|---|
| In vivo |
L'hinokitiol réduit la croissance tumorale, potentiellement par l'atténuation de la tumorigenicité, et induit des dommages à l'DNA et l'autophagie pour supprimer la progression tumorale. Une étude in vivo démontre que le traitement à l'hinokitiol réduit significativement le nombre total de nodules métastatiques pulmonaires chez la souris et améliore les altérations histologiques chez les souris C57BL/6 injectées avec B16-F10.
|
Références |
|
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
