pour la recherche uniquement
Clofibric Acid PPAR agoniste
Réf. CatalogueS4207
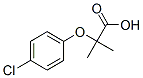
Structure chimique
Poids moléculaire: 214.65
Contrôle Qualité
- Cité dans Nature Medicine pour sa qualité supérieure
- COA
- NMR
- HPLC
- SDS
- Fiche technique
| Cibles apparentées | Dehydrogenase HSP Transferase P450 (e.g. CYP17) PDE phosphatase Vitamin Carbohydrate Metabolism Mitochondrial Metabolism Drug Metabolite |
|---|---|
| Autre PPAR Inhibiteurs | T0070907 GW9662 GW6471 WY-14643 (Pirinixic Acid) GSK3787 GW0742 AZ6102 Harmine Astaxanthin Eupatilin |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 214.65 | Formule | C10H11ClO3 |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 882-09-7 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | Chlorofibrinic acid | Smiles | CC(C)(C(=O)O)OC1=CC=C(C=C1)Cl | ||
Solubilité
|
In vitro |
DMSO
: 43 mg/mL
(200.32 mM)
Ethanol : 43 mg/mL Water : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
PPARα
|
|---|---|
| In vitro |
Clofibric Acid augmente l'expression génique du CYP4A6 dans les cellules RK13 transfectées avec PPAR-G avec une EC50 de 80 μM. Le traitement par Clofibric Acid (1 mM) pendant 4 jours induit une augmentation de 500 fois de l'ARN P450 4Al et une augmentation de 280 fois de l'acyl-CoA oxydase et de l'ARN P450 2Bl dans les hépatocytes, par rapport aux cultures témoins. Clofibric Acid (250 μM) induit une régulation positive des gènes impliqués dans la prolifération des peroxysomes et dans la prolifération cellulaire, ainsi qu'une régulation négative des gènes impliqués dans l'apoptose dans les hépatocytes de rongeurs. Le traitement par Clofibric Acid est capable de provoquer une régulation positive du gène de la protéine de liaison aux acides gras L (L-FABP) dans les hépatocytes d'origine rongeur et humaine. Clofibric Acid régule également positivement l'expression des gènes des voies cytosolique, microsomale et mitochondriale impliquées dans le transport et le Metabolism des acides gras dans les cultures d'hépatocytes de rongeurs et humains, et augmente le niveau des gènes de la voie peroxysomale du Lipid Metabolism chez les rongeurs. Une régulation positive du facteur nucléaire hépatocytaire 1α (HNF 1α) par Clofibric Acid est observée dans les cultures d'hépatocytes humains. Clofibric Acid inhibe également de manière dose-dépendante la prolifération cellulaire des cellules OVCAR-3 et DISS cultivées dérivées du cancer ovarien humain. Le traitement par Clofibric Acid augmente l'expression de la carbonyl réductase, qui favorise la conversion de la prostaglandine E2 (PGE2) en PGF 2α. |
| In vivo |
Le traitement par Clofibric Acid (50 mg/kg) pendant 4 jours par gavage induit l'expression de P450 4A et de BFB dans les zones 3 et 2 de l'acinus hépatique chez les rats. 300 mg/kg de Clofibric Acid provoquent une forte coloration des deux protéines dans tout l'acinus hépatique. Le traitement par Clofibric Acid (9 000 ppm) dans l'alimentation supprime significativement la croissance des tumeurs OVCAR-3 xénotransplantées s.c. (46 %) et prolonge significativement la survie des souris atteintes d'ascites malignes dérivées de cellules DISS par rapport au contrôle. Le traitement par Clofibric Acid augmente l'expression de la carbonyl réductase in vivo. Le traitement par Clofibric Acid diminue le niveau de PGE2 ainsi que la quantité de facteur de croissance endothélial vasculaire (VEGF) dans les tumeurs OVCAR-3 et les ascites dérivées de DISS. Une densité de microvaisseaux réduite et une apoptose induite sont observées dans les tumeurs solides OVCAR-3 traitées par Clofibric Acid. |
Références |
|
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
