pour la recherche uniquement
WY-14643 (Pirinixic Acid) PPAR activateur
Réf. CatalogueS8029
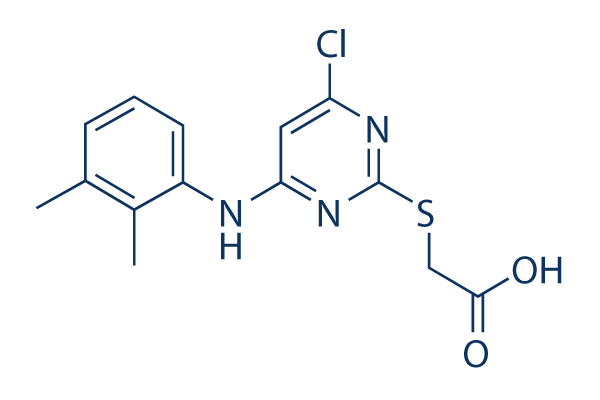
Structure chimique
Poids moléculaire: 323.8
Contrôle Qualité
| Cibles apparentées | Dehydrogenase HSP Transferase P450 (e.g. CYP17) PDE phosphatase Vitamin Carbohydrate Metabolism Mitochondrial Metabolism Drug Metabolite |
|---|---|
| Autre PPAR Inhibiteurs | T0070907 GW9662 GW6471 GSK3787 GW0742 AZ6102 Harmine Astaxanthin Eupatilin GSK0660 |
Culture cellulaire, traitement et concentration de travail
| Lignées cellulaires | Type dessai | Concentration | Temps dincubation | Formulation | Description de lactivité | PMID |
|---|---|---|---|---|---|---|
| Hep G2 cells | Function assay | Agonist activity at mouse PPARalpha ligand binding domain expressed in human Hep G2 cells co-transfected with Gal4-DBD by luciferase reporter gene assay, EC50=0.04 μM | ||||
| MCF7 cells | Function assay | Agonist activity at human PPARalpha expressed in MCF7 cells co-transfected CPTI DR1-type RE after 6 hrs by luciferase reporter gene assay, EC50=0.542 μM | ||||
| U2OS cells | Function assay | Agonist activity at human PPARalpha in U2OS cells by transactivation assay, EC50=12 μM | ||||
| HEK293 cells | Function assay | Agonist activity at human PPARalpha expressed in HEK293 cells cotransfected with PPREx4-TK-luc assessed as activation of luciferase activity measured after 48 hrs by transactivation assay, EC50=23.33 μM | ||||
| COS7 cells | Function assay | Activation of human PPARalpha ligand binding domain expressed in COS7 cells by luciferase reporter gene assay, IC50=36.3 μM | ||||
| EAhy926 cells | Function assay | 10 uM | 12 h | Inhibition of tube formation in human EAhy926 cells at 10 uM pre-incubated for 12 hrs measured after 24 hrs by phase-contrast microscopy | ||
| mouse NIH3T3 cells | Function assay | 0.1-10 μM | Transactivation of mouse recombinant PPARalpha expressed in mouse NIH3T3 cells at 0.1 uM to 10 uM by PPRE activation based dual luciferase reporter gene assay relative to control | |||
| HepaR cells | Function assay | 25 μM | 1 day | Agonist activity at PPARalpha in human HepaR cells assessed as increase in HMGCS2 gene expression at 25 uM incubated for 1 day by quantitative PCR method relative to untreated control | ||
| Cliquez pour voir plus de données expérimentales sur la lignée cellulaire | ||||||
Informations chimiques, stockage et stabilité
| Poids moléculaire | 323.8 | Formule | C14H14ClN3O2S |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 50892-23-4 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | NSC 310038 | Smiles | CC1=C(C(=CC=C1)NC2=CC(=NC(=N2)SCC(=O)O)Cl)C | ||
Solubilité
|
In vitro |
DMSO
: 64 mg/mL
(197.65 mM)
Ethanol : 64 mg/mL Water : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
PPARα
1.5 μM(EC50)
|
|---|---|
| In vitro |
Le WY 14643 (10 μM) inhibe presque complètement la production d'interleukine-6 et de prostaglandine induite par l'interleukine-1, ainsi que l'expression de la cyclooxygénase-2 dans les cellules musculaires lisses aortiques, par la répression de la signalisation NF-κB. Le WY14643 (250 μM) réduit significativement les niveaux d'expression de VCAM-1, à 52 % des cellules endothéliales humaines stimulées par le TNF-α. Le prétraitement des cellules endothéliales avec le WY 14643 (10 μM) avant la stimulation par le TNF-α réduit l'adhésion des cellules U937 de 50 %. |
| In vivo |
L'administration de WY 14643 (1 mg/kg en bolus i.v.) 30 min avant l'occlusion de l'artère descendante antérieure gauche, entraîne une réduction significative de la taille de l'infarctus d'environ 44 % chez les rats soumis à une ischémie myocardique régionale (25 min) et à une reperfusion (2 h). Le WY 14643 (3 mg/kg) abaisse les niveaux plasmatiques basaux de glucose, de triglycérides (-16 % vs non traités), et de leptine (-52 %), ainsi que les triglycérides musculaires (-34 %) et les acyl-CoA à longue chaîne totaux (LCACoAs) (-41 %) chez les rats nourris avec un régime riche en graisses. Le WY14643 réduit considérablement le poids de la graisse viscérale et la teneur totale en triglycérides hépatiques sans augmenter la prise de poids corporel. Le WY14643 améliore la sensibilité à l'insuline de tout le corps (le taux d'infusion de glucose par clamp augmente de 35 % et la disposition du glucose de 22 %, vs non traités). Le WY 14643 améliore l'indice métabolique du glucose musculaire (Rg') médié par l'insuline dans les muscles rouges (47 %) et blancs (63 %) ainsi que dans le tissu adipeux blanc (90 %), et réduit l'accumulation de triglycérides musculaires et de LCACoA. |
Références |
|
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
