pour la recherche uniquement
Taurochenodeoxycholic acid Caspase activateur
Réf. CatalogueS3865
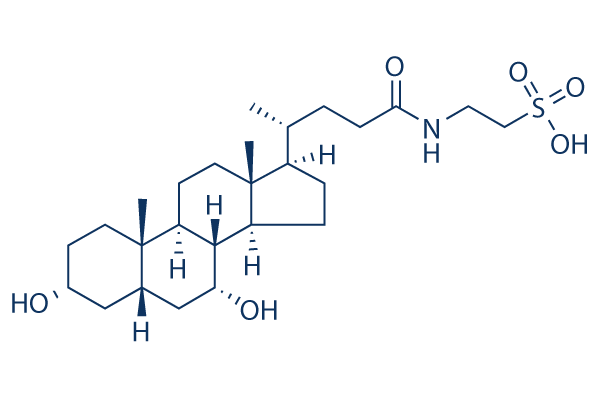
Structure chimique
Poids moléculaire: 499.70
Contrôle Qualité
| Cibles apparentées | Bcl-2 PD-1/PD-L1 Ferroptosis p53 Apoptosis related Synthetic Lethality STAT TNF-alpha Ras KRas |
|---|---|
| Autre Caspase Inhibiteurs | Emricasan (IDN-6556) Z-VAD-FMK Q-VD-Oph Z-DEVD-FMK Belnacasan (VX-765) Z-IETD-FMK Ac-DEVD-CHO Z-LEHD-FMK TFA Z-VAD(OH)-FMK PAC-1 |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 499.70 | Formule | C26H45NO6S |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 516-35-8 | -- | Stockage des solutions mères |
|
|
| Synonymes | Taurochenodeoxycholate, TCDCA, 12-Deoxycholyltaurine, Chenodeoxycholyltaurine, Chenyltaurine | Smiles | CC(CCC(=O)NCCS(=O)(=O)O)C1CCC2C1(CCC3C2C(CC4C3(CCC(C4)O)C)O)C | ||
Solubilité
|
In vitro |
DMSO
: 100 mg/mL
(200.12 mM)
Water : 100 mg/mL Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| In vitro |
Taurochenodeoxycholic acid (TUDCA) induit la dissociation des CSH CD34+ des cellules stromales en diminuant l'expression des molécules d'adhésion. Il induit la mobilisation des cellules souches de la moelle osseuse et leur différenciation en cellules progénitrices endothéliales (CPE) et améliore la prolifération, l'invasion et la formation de tubes des CPE via l'activation d'Akt et d'ERK. Le TCDCA induit le processus d'Apoptosis par l'activation de la cascade de Caspase dans les macrophages, et ce processus pourrait être impliqué dans la voie de signalisation PKC/JNK.
|
|---|---|
| In vivo |
Le TUDCA a des effets neuroprotecteurs dans les cultures neuronales et des effets positifs sur la reperfusion d'ischémie dans les modèles animaux, réduisant la zone d'infarctus et l'inflammation via l'atténuation du stress du réticulum endoplasmique (RE). Le TUDCA est incorporé dans les cellules cibles via le transporteur d'anions organiques (OATP) 2, OATP8 et le polypeptide de cotransport Na+-taurocholate (NTCP). Le TUDCA inhibe l'hyperplasie néo-intimale en favorisant l'Apoptosis des cellules musculaires lisses via l'induction de l'expression de la MAP kinase phosphatase-1 (MKP-1). De plus, le TUDCA protège les hépatocytes et restaure l'homéostasie du glucose en réduisant le stress du RE. Le TUDCA améliore la néovascularisation in vivo. Le TCDCA à des doses de 0,05 et 0,1 g/kg peut réduire de manière extrêmement significative le coefficient pulmonaire chez les souris modèles. Le TCDCA à une dose de 0,2 g/kg réduit significativement le coefficient pulmonaire chez les souris modèles (P<0,05) ; le TCDCA à des doses de 0,05 et 0,1 g/kg réduit significativement les dommages pathologiques de leurs poumons ; le TCDCA peut réduire de manière extrêmement significative les niveaux d'expression de TNF-α et de TIMP-2 dans les tissus pulmonaires chez les souris atteintes de fibrose pulmonaire (P>0,01), le niveau d'expression de MMP-9 a augmenté de manière extrêmement significative (P>0,01), alors qu'il n'a pas d'effets significatifs sur MMP2. Ainsi, le TCDCA a des actions antagonistes sur la fibrose pulmonaire chez les souris.
|
Références |
|
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
